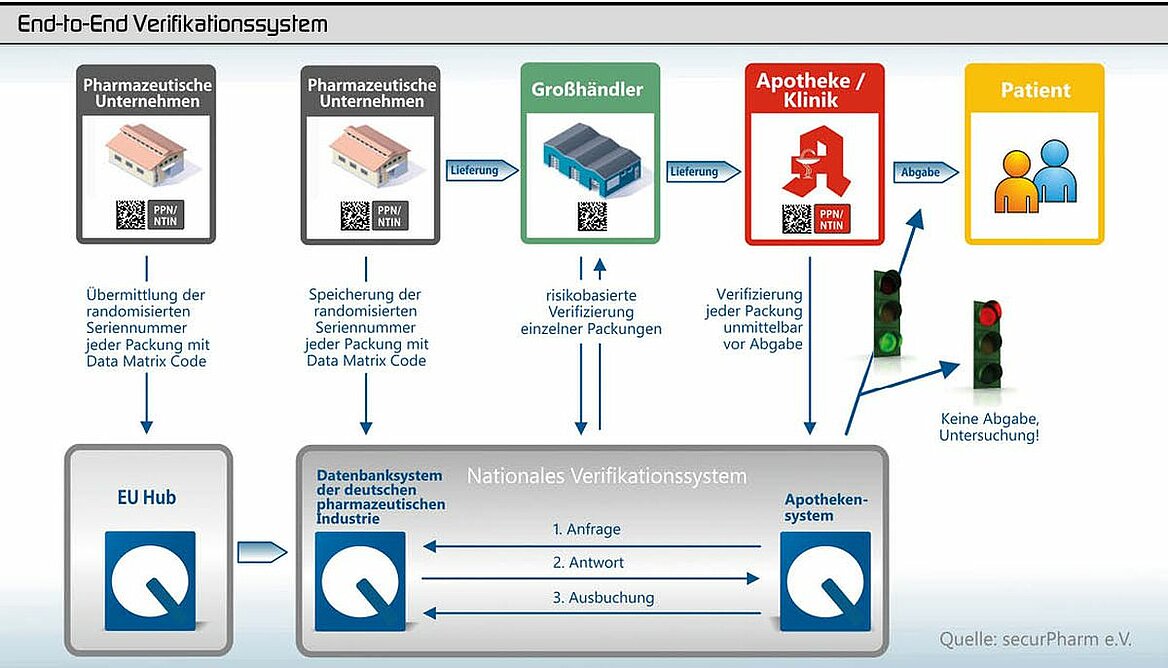
Die Umsetzung der EU-Richtlinie zum Fälschungsschutz für Pharmaverpackungen scheint in Deutschland auf dem Weg zu sein. Ab dem Stichtag 9. Februar 2019 können verschreibungspflichtige Medikamente vom Hersteller dann nur noch mit einem individuellen Erkennungsmerkmal, einer Seriennummer sowie einem Erstöffnungsschutz für den Handel freigegeben werden.
Zahlreiche Produzenten von Pharmaverpackungen haben sich bereits auf die neuen Anforderungen eingestellt. Beobachter sind zuversichtlich, dass es gelingen wird, bis zum Stichtag ein funktionierendes Sicherheitssystem aufzubauen.
Nathalie Steinhauser, Sprecherin der zuständigen Organisation securPharm, Frankfurt am Main, erklärte gegenüber dem EUWID: „Wir kommen mit dem Aufbau des neuen Fälschungsschutzes gut voran. Bis zum 9. Februar 2019 wird es uns gelingen, ein funktionierendes Sicherheitssystem in Deutschland aufzubauen."
Schutz bietet unter anderem die Kontrolle der Vertriebswege. Laut EU-Verordnung Nr. 2016/161 sollen deshalb verschreibungspflichtige Arzneimittel auf ihrer Verpackung in Zukunft mit Sicherheitsmerkmalen versehen sein. Der zeitliche Rahmen zur Umsetzung beträgt drei Jahre.
Stichtag 9. Februar 2019
Stichtag ist wie bereits erwähnt der 9. Februar 2019. Ab diesem Zeitpunkt können verschreibungspflichtige Medikamente vom Hersteller nur noch mit einem individuellen Erkennungsmerkmal, einer Seriennummer sowie einem Erstöffnungsschutz für den Handel freigegeben werden. Die etwa 20.000 Apotheken in Deutschland dürfen Arzneimittel dann nur noch nach erfolgreicher Echtheitsprüfung verkaufen.
securPharm e.V. ist die deutsche Organisation für diese Prüfung von Arzneimitteln. Ihre Aufgabe ist es, das Kontrollsystem aufzubauen und zu betreiben. Dessen technische Umsetzung liegt in der Verantwortung der ACS PharmaProtect GmbH, Berlin. Etwa 200 von insgesamt 400 betroffenen Herstellern in Deutschland haben sich securPharm inzwischen angeschlossen (Stand Dezember 2017).
Deutschland: Vorreiter im Fälschungsschutz
„Im europäischen Vergleich liegt Deutschland mit der Umsetzung der Fälschungsrichtlinie weit vorn“, betont Nathalie Steinhauser und fährt fort: „Der Ausblick auf andere EU-Mitgliedstaaten des europäischen Wirtschaftsraumes (EWR) stimmt optimistischer als noch zu Jahresanfang 2017. Inzwischen haben sich in 25 dieser Länder sowie in der Schweiz, die sich auf freiwilliger Basis beteiligt, die nationalen Organisationen gegründet, die die jeweiligen Systeme für die Echtheitsprüfung aufbauen“.
Dieter Mößner, Projekt Engineer Pharma beim Verpackungsspezialisten Edelmann, Heilbronn, erklärte hierzu gegenüber dem EUWID: „EU-weit ist Deutschland sehr weit, viele Länder sind jedoch noch nicht so weit. Es wird ein hartes Stück Arbeit werden, bis alle EU-Länder, alle betroffenen PUs (Pharmaunternehmen) ihre Arzneimittel FMD-konform kennzeichnen und auch die Datenbank- und Apothekensysteme arbeiten.“
Den gesamten Beitrag zum Thema Fälschungsschutz von Pharma-Verpackungen aus EUWID VP 01/2018 erhalten Abnonnenten hier.